Stratégies nanotechnologiques pour le traitement des tumeurs cérébrales de haut grade
Pourquoi s’intéresser aux tumeurs cérébrales de haut grade ?
Une tumeur est définie comme une situation pathologique dans laquelle une prolifération incontrôlée de cellules survient au sein d’un tissu ou d’un organe sain.
Tous les organes des mammifères sont susceptibles d’être le siège du développement d’une telle pathologie, le cerveau comme les autres, malgré ses protections naturelles (boîte crânienne, présence de la barrière hémato-encéphalique).
D’une manière simplifiée, on peut classifier les tumeurs en :
Nous avons choisi de nous intéresser aux tumeurs cérébrales primaires de grade 411 pour plusieurs raisons :
Pour un pays comme le Canada, cela représentait 1,850 décès en 2012.
Comment les diagnostique-t-on ? Avec quels outils ?
Les symptômes classiques incluent des maux de tête, des paralysies et des troubles locomoteurs.
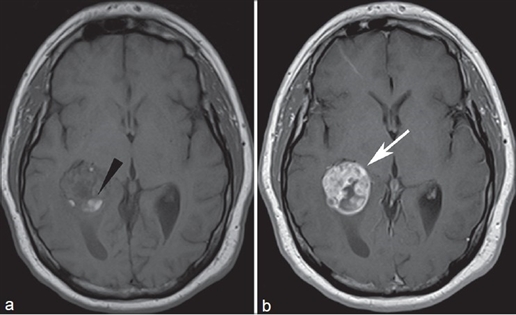
Les patients sont diagnostiqués via des examens d’imagerie médicale, principalement par IRM (Imagerie de Résonance Magnétique). Cette technique de très bonne résolution est malheureusement peu sensible. Il faut donc administrer aux patients de grandes quantités d’agents de contraste (CA, figure 1).
Figure 1. Coupe transversale en IRM d’un cerveau de patient souffrant d’une lésion cérébrale de type cancéreux. a : image obtenue sans agent de contraste; b : image observée après injection d’un agent de contraste (complexe de Gd(III)). Figure 8 de la publication de Fink et Fink, 20132.
Stratégie thérapeutique actuelle et causes de son échec
Stratégie thérapeutique actuelle3 :
Causes de l’échec thérapeutique3 :
En quoi les nanotechnologies peuvent-elles aider ?
L'objectif des nanotechnologies consiste à produire des objets ou matériaux dont une des dimensions est comprise dans l’intervalle nanométrique (de 1à 999 nm, soit 10-9 m).
Dans le domaine pharmaceutique, on utilise ce concept pour produire des vecteurs de médicaments, capables de transporter, en les protégeant, de grandes quantités d’actifs thérapeutiques ou diagnostiques.
Les avantages sont multiples :
Objectif de notre programme
Concevoir des nano-objets permettant le diagnostic préopératoire précis et / ou le traitement des tumeurs cérébrales les plus agressives.
Pour atteindre cet objectif, nous avons identifié trois projets :
2Fink KR, Fink JR. Imaging of brain metastases. Surg Neurol Int 2013;4, Suppl S4:209-19
3A. Ghose G. Lim, S. Husain, Treatment for glioblastoma multiforme: current guidelines and Canadian practice, Curr Oncol. 2010, 17(6): 52–58 ; J.C. Easaw et al., for the Canadian Glioblastoma Recommendations Committee, Canadian recommendations for the treatment of recurrent or progressive glioblastoma multiforme, Curr Oncol. 2011, 18(3): e126–e136.
4M. Callewaert et al., Etoposide encapsulation in surface-modified poly(lactide-co-glycolide) nanoparticles strongly enhances glioma antitumor efficiency, J Biomed Mater Res A. 2013, 101(5):1319-27
5T. Courant et al., Hydrogels incorporating GdDOTA: towards highly efficient dual T1/T2 MRI contrast agents. Angew Chem Int Ed Engl. 2012, 51(36):9119-22; M. Callewaert et al. Tuning the composition of biocompatible Gd nanohydrogels to achieve hypersensitive dual T 1/T 2 MRI contrast agents. Journal of Materials Chemistry B. 2014, 2(37): 6397-6405.
Une tumeur est définie comme une situation pathologique dans laquelle une prolifération incontrôlée de cellules survient au sein d’un tissu ou d’un organe sain.
Tous les organes des mammifères sont susceptibles d’être le siège du développement d’une telle pathologie, le cerveau comme les autres, malgré ses protections naturelles (boîte crânienne, présence de la barrière hémato-encéphalique).
D’une manière simplifiée, on peut classifier les tumeurs en :
- tumeurs non cancéreuses (bégnines). Elles sont caractérisées par un développement lent, localisé et n’ont pas tendance à envahir les tissus lointains, ni à récidiver après traitement. On les qualifie généralement de stade de développement (= grade) 1 ou 2.
Dans le cas des tumeurs cérébrales, on compte les chordomes (issus des cellules embryonnaires de la moelle épinière ou à la base du nerf crânien), les hémangioblastomes (tumeurs des vaisseaux sanguins), les méningiomes (tumeurs des méninges), les ostéomes (apparaissant dans les os du crâne), les pinéalomes (tumeurs de la glande pinéale), les adénomes hypophysaires (issus de l'hypophyse) et les schwannomes (naissant au sein des cellules de Schwann).
- tumeurs cancéreuses (malignes). Elles sont caractérisées un développement rapide, en accélération et s’étendent aux tissus environnants, ainsi que plus lointains (métastases). On les qualifie généralement de stade de développement 3 ou 4.
Dans le cas des tumeurs cérébrales, on compte les astrocytomes anaplasiques (qui touchent les astrocytes), les oligodendrogliomes (issus des oligodendrogliocytes), les épendymomes et les gangliogliomes de haut grade.
Nous avons choisi de nous intéresser aux tumeurs cérébrales primaires de grade 411 pour plusieurs raisons :
- dans les pays dits ‘industrialisés’, ces tumeurs extrêmement malignes touchent environ 3 adultes sur 100,000.
Pour un pays comme le Canada, cela représentait 1,850 décès en 2012.
- à l’heure actuelle, il n’existe pas de traitement efficace. La survie médiane est de 14.6 mois après le diagnostic et malgré les traitements.
Comment les diagnostique-t-on ? Avec quels outils ?
Les symptômes classiques incluent des maux de tête, des paralysies et des troubles locomoteurs.
Les patients sont diagnostiqués via des examens d’imagerie médicale, principalement par IRM (Imagerie de Résonance Magnétique). Cette technique de très bonne résolution est malheureusement peu sensible. Il faut donc administrer aux patients de grandes quantités d’agents de contraste (CA, figure 1).
Figure 1. Coupe transversale en IRM d’un cerveau de patient souffrant d’une lésion cérébrale de type cancéreux. a : image obtenue sans agent de contraste; b : image observée après injection d’un agent de contraste (complexe de Gd(III)). Figure 8 de la publication de Fink et Fink, 20132.
Stratégie thérapeutique actuelle et causes de son échec
Stratégie thérapeutique actuelle3 :
- Dès que cela est possible, la chirurgie est le premier traitement proposé. L’objectif est de réduire le plus possible la masse de la tumeur à traiter. En effet, dans le cas des tissus cérébraux, la chirurgie est une option à envisager si la zone tumorale est atteignable sans mettre la vie du patient en danger. Cela signifie que cette option n’est pas disponible pour les tumeurs se développant dans les zones profondes ou sensibles du cerveau.
- La radio- et/ou chimiothérapie sont généralement initiées après la chirurgie. Ces traitements ont pour objectif d’éliminer les cellules de la tumeur restantes et de limiter le risque de récidive. Compte tenu de l’agressivité de ce type de tumeurs, les cliniciens vont plutôt utiliser des ‘cocktails’ médicamenteux que des drogues seules. La substance active la plus prescrite actuellement, pour les GBM, est le témozolomide.
Causes de l’échec thérapeutique3 :
- Il s’agit de tumeurs ‘silencieuses’, récidivantes (± 2 cm de zone d’exérèse chirurgicale), hétérogènes. Généralement les premiers symptômes apparaissent alors que la tumeur a déjà atteint la taille d’une noix, souvent d’une petite orange…
- Présence de la Barrière Hémato-Encéphalique (BHE), structure complexe de cellules endothéliales hyper-jointives qui empêche plus de 98 % des molécules thérapeutiques d’atteindre le tissu cérébral.
En quoi les nanotechnologies peuvent-elles aider ?
L'objectif des nanotechnologies consiste à produire des objets ou matériaux dont une des dimensions est comprise dans l’intervalle nanométrique (de 1à 999 nm, soit 10-9 m).
Dans le domaine pharmaceutique, on utilise ce concept pour produire des vecteurs de médicaments, capables de transporter, en les protégeant, de grandes quantités d’actifs thérapeutiques ou diagnostiques.
Les avantages sont multiples :
- Diminuer les quantités de substances actives introduites dans l’organisme : les nanovecteurs ont tendance à s’accumuler naturellement dans les zones tumorales, plutôt que de se distribuer à tout l’organisme comme les substances actives ‘libres’. Cela doit permettre d’augmenter l’efficacité localement, en diminuant les effets secondaires souvent néfastes de ces traitements.
- Introduire et transporter des molécules actives qui ne possèdent pas de propriétés physicochimiques favorables (par exemple, qui ne sont pas solubles dans l’eau et les milieux biologiques).
- Assurer un transport au travers des barrières naturelles de l’organisme.
Objectif de notre programme
Concevoir des nano-objets permettant le diagnostic préopératoire précis et / ou le traitement des tumeurs cérébrales les plus agressives.
Pour atteindre cet objectif, nous avons identifié trois projets :
- Projet 1 - synthétiser des nanogels théranostiques :
Il s’agit de concevoir, réaliser et caractériser l’efficacité de nano-structures qui transporteront à la fois des agents thérapeutiques et diagnostiques . Ainsi pourrait-on vérifier que le médicament atteint bien la zone cible et visualiser les effets sur la croissance de la tumeur en temps réel.
- Projet 2 - synthétiser des nanoparticules polymériques ‘intelligentes’ :
Par l’emploi d’un revêtement de surface adéquat, le passage de la BHE (barrière hémato-encéphalique) pourrait être favorisé. Après le transport des nanovecteurs de l’autre côté de cette barrière, une fois rendu dans le cerveau, ce revêtement se détacherait et permettrait de dévoiler des molécules d’attache spécifiques aux cellules tumorales. Ainsi les agents diagnostiques et / ou les molécules thérapeutiques seraient-elles dirigées spécialement vers les cellules malades.
- Projet 3 – un modèle pertinent de la BHE :
Prévoir efficacement à quel point les substances actives nouvellement découvertes ou les nanovecteurs peuvent traverser la BHE est un défi majeur pour le traitement des tumeurs cérébrales, mais également pour beaucoup de maladies touchant les tissus cérébraux. Nous nous proposons de réaliser un modèle multicellulaire validé à cet effet.
1W.P. Mason et al., for the Canadian GBM Recommendations Committe, Canadian recommendations for the treatment of glioblastoma multiforme, Curr Oncol. 2007, 14(3): 110–117.
2Fink KR, Fink JR. Imaging of brain metastases. Surg Neurol Int 2013;4, Suppl S4:209-19
3A. Ghose G. Lim, S. Husain, Treatment for glioblastoma multiforme: current guidelines and Canadian practice, Curr Oncol. 2010, 17(6): 52–58 ; J.C. Easaw et al., for the Canadian Glioblastoma Recommendations Committee, Canadian recommendations for the treatment of recurrent or progressive glioblastoma multiforme, Curr Oncol. 2011, 18(3): e126–e136.
4M. Callewaert et al., Etoposide encapsulation in surface-modified poly(lactide-co-glycolide) nanoparticles strongly enhances glioma antitumor efficiency, J Biomed Mater Res A. 2013, 101(5):1319-27
5T. Courant et al., Hydrogels incorporating GdDOTA: towards highly efficient dual T1/T2 MRI contrast agents. Angew Chem Int Ed Engl. 2012, 51(36):9119-22; M. Callewaert et al. Tuning the composition of biocompatible Gd nanohydrogels to achieve hypersensitive dual T 1/T 2 MRI contrast agents. Journal of Materials Chemistry B. 2014, 2(37): 6397-6405.
Les glioblastomes multiformes sont les formes de grade 4 des astrocytomes et sont les plus agressifs et malheureusement les plus fréquents chez l’adulte.